🧪 화학식량과 몰 (원자량, 분자량, 화학식량, 몰)
1. 원자량 (Atomic Mass)의 정의
- 원자량은 몰(mol) 개념을 이해하기 위한 첫 번째 단계이며 가장 중요한 기초 개념이다.
- 원자량은 상대적인 질량 개념이다.
- 기준: 질량수가 12인 탄소 원자의 질량을 정확히 12로 정하고, 이를 기준으로 삼아 다른 원자들의 질량을 나타낸 값이다.
2. 질량수 (Mass Number)와 원자의 질량
- 원자의 질량은 원자핵(양성자+중성자)과 전자로 구성되지만, 전자의 질량은 양성자나 중성자에 비해 약 2천 배 가까이 매우 가볍다.
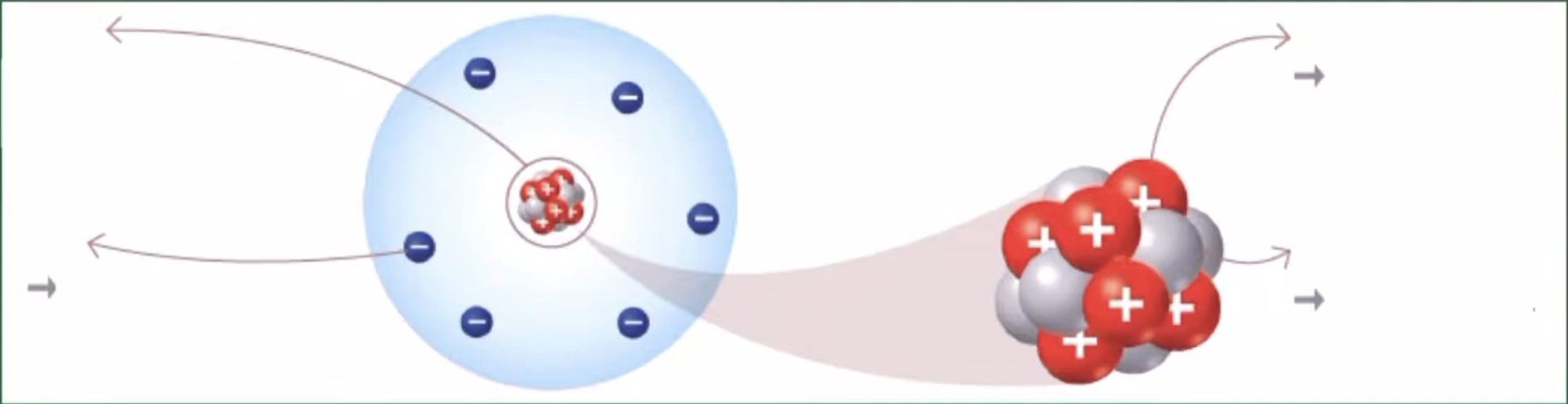
- 따라서 원자의 질량을 결정하는 주된 입자는 양성자와 중성자이다.

- 질량수는 원자핵을 구성하는 양성자 수와 중성자 수의 합으로 정의된다. (질량을 결정하는 입자의 수).
- 표기: 원소 기호의 왼쪽 위에 질량수를 표시하며, 왼쪽 아래에는 원자 번호(양성자 수)를 표시한다.
- 예시: 나트륨($^{23}_{11}\text{Na}$)은 원자 번호 11번(양성자 11개), 질량수 23이므로 중성자는 $23 - 11 = 12$개이다.
3. 원자량 개념 도입의 필요성
- 실제 원자 한 개의 질량은 $10^{-23} \text{g}$처럼 매우 작아 일상생활에서 다루기 어렵고, 실제 질량 값으로는 원자 간의 질량 차이(몇 배 무거운지 등)를 직관적으로 비교하기 힘들다.
- 질량수 12인 탄소의 실제 질량을 $12.00$이라는 간단한 숫자로 약속하고, 이를 기준으로 다른 원소의 질량을 상대값으로 표현함으로써, 숫자가 간단해지고 원자 간의 질량 비교(대소, 배수)가 용이해진다.
4. 주요 원소의 원자량 (평균 원자량)
- 탄소를 12로 정했을 때, 다른 원소들의 원자량은 다음과 같다.
- 수소(H): 1
- 탄소(C): 12
- 질소(N): 14
- 산소(O): 16
- 나트륨(Na): 23
- 황(S): 32
- 염소(Cl): 35.5
- 칼륨(K): 39
- 칼슘(Ca): 40
- 평균 원자량: 염소의 원자량이 35.5인 것과 같이, 소수점으로 나타나는 원자량은 실제로 그 원자량을 갖는 원자가 존재하는 것이 아니다. 이는 질량수가 다른 동위 원소들($^{35}\text{Cl}$, $^{37}\text{Cl}$ 등)이 자연계에 존재하는 비율까지 고려하여 계산한 평균값이다. (예: 염소의 경우 35짜리와 37짜리가 3:1의 비율로 존재).
- 암기: 문제에서 원자량을 제시하지만, 수소(1), 탄소(12), 질소(14), 산소(16), 염소(35.5) 등은 암기해 두면 문제 풀이 시간을 절약할 수 있다.

- 원자량 대략 계산법 (참고):
- 원자 번호(n)가 짝수일 경우: 약 2n
- 원자 번호(n)가 홀수일 경우: 약 2n+1
- 예외: 홀수 원소 중 수소(H)와 질소(N)는 예외이다.
5. 분자량과 화학식량 (Molecular/Formula Mass)
- 분자량: 분자를 구성하는 모든 원자들의 원자량을 합한 값이다. (분자에만 사용 가능).
- 화학식량: 물질의 화학식을 이루는 각 원자들의 원자량을 합한 값이다. (분자, 이온 결합 물질 등 모든 물질에 사용 가능).
- 실용적 구분:
- 분자량은 분자(공유 결합 물질)에만 사용할 수 있다.
- 화학식량은 분자가 아닌 이온 결합 물질($\text{NaCl}$, $\text{CaCO}_3$, $\text{NaOH}$) 등에도 사용할 수 있다.
- 혼동을 피하고 서술형에서 감점당하지 않기 위해, 모든 물질의 화학식으로 계산한 질량은 화학식량으로 통일하여 표현하는 것이 안전하다.
| 화학식 | 이름 | 계산 | 화학식량 |
|---|---|---|---|
| $\text{H}_2\text{O}$ | 물 | $1 \times 2 + 16$ | 18 |
| $\text{NH}_3$ | 암모니아 | $14 + 1 \times 3$ | 17 |
| $\text{CH}_4$ | 메테인 | $12 + 1 \times 4$ | 16 |
| $\text{CO}_2$ | 이산화 탄소 | $12 + 16 \times 2$ | 44 |
| $\text{NaCl}$ | 염화 나트륨 | $23 + 35.5$ | 58.5 |
| $\text{CaCO}_3$ | 탄산 칼슘 | $40 + 12 + 16 \times 3$ | 100 |
| $\text{NaOH}$ | 수산화 나트륨 | $23 + 16 + 1$ | 40 |
- 단위: 원자량, 분자량, 화학식량은 모두 기준(탄소=12)을 정해 나타낸 상대적인 값이므로, 기본적으로 단위가 없다. (다만, 원자 질량 단위인 amu를 사용하기도 한다).
6. 몰 (Mole)의 정의 및 개념
- 몰은 연필을 세는 '다스'(12자루)나 인삼을 세는 '채'(100뿌리)처럼, 입자의 개수를 세기 위해 만든 묶음 단위이다.
- 몰은 원자, 분자, 이온 등 매우 작은 입자들의 양을 나타내기 위해 사용된다.

7. 1몰의 기준: 아보가드로 수 ($\text{N}_{\text{A}}$)
- $\mathbf{1 \text{ mol}}$은 입자 $6.02 \times 10^{23}$ 개를 의미하며, 이 숫자를 아보가드로 수($\mathbf{\text{N}_{\text{A}}}$)라고 부른다.
아보가드로 수가 등장한 이유 (몰의 정의 배경)
- 몰($1 \text{ mol}$)이라는 개수를 $6.02 \times 10^{23}$으로 정한 것은 원자량의 정의에서 출발한다.
- 과학자들은 원자량에 그램(g)을 붙인 질량 속에 들어있는 입자의 개수를 기준으로 삼았다.
- 기준: 질량수가 12인 탄소 원자($\text{C}$)의 원자량은 12이다.
- 탄소 원자를 원자량 값에 $\text{g}$을 붙인 $12 \text{ g}$ 만큼 준비했을 때, 그 안에 들어있는 탄소 원자의 개수가 정확히 $\mathbf{6.02 \times 10^{23} \text{ 개}}$임을 확인했다.
- 이 개수를 $1 \text{ mol}$ 로 약속한 것이다.
몰과 질량의 관계
- 모든 물질은 화학식량(또는 분자량)에 $\text{g}$을 붙인 질량만큼 있으면 항상 $1 \text{ mol}$ 이다.
- 예: 수소(H) 원자량 1 $\rightarrow 1 \text{ g} = 1 \text{ mol} = 6.02 \times 10^{23}$ 개
- 예: 산소($\text{O}$) 원자량 16 $\rightarrow 16 \text{ g} = 1 \text{ mol} = 6.02 \times 10^{23}$ 개
- 예: 물($\text{H}_2\text{O}$) 분자량 18 $\rightarrow 18 \text{ g} = 1 \text{ mol} = 6.02 \times 10^{23}$ 개의 $\text{H}_2\text{O}$ 분자
8. 몰을 활용한 계산 원리
- 몰 관련 문제 풀이의 핵심은 1몰을 항상 기준으로 잡고, 주어진 양이 기준의 몇 배인지 파악하여 계산하는 것이다.
질량 $\leftrightarrow$ 몰 수 (예시)
- 물($\text{H}_2\text{O}$, 분자량 18) $36 \text{ g}$:
- 기준: $18 \text{ g} = 1 \text{ mol}$
- $36 \text{ g}$은 기준의 2배이므로 $\mathbf{2 \text{ mol}}$ 이다.
- 메테인($\text{CH}_4$, 분자량 16) $0.5 \text{ mol}$:
- 기준: $1 \text{ mol} = 16 \text{ g}$
- $0.5 \text{ mol}$은 절반이므로 $\mathbf{8 \text{ g}}$ 이다.
구성 원자의 몰 수 계산 (예시)
- 이산화 탄소($\text{CO}_2$, 화학식량 44) $44 \text{ g}$에 포함된 산소(O) 원자의 몰 수:
- $\text{CO}_2$ $44 \text{ g}$은 $\text{CO}_2$ $\mathbf{1 \text{ mol}}$이다.
- $\text{CO}_2$ 분자 1개에는 $\text{O}$ 원자가 2개 들어있다.
- 따라서 $\text{CO}_2$ $1 \text{ mol}$에는 $\text{O}$ 원자가 $1 \times 2 = \mathbf{2 \text{ mol}}$ 만큼 들어있다.
- 암모니아($\text{NH}_3$, 분자량 17)에 들어있는 수소(H) 원자의 질량이 $6 \text{ g}$일 때, $\text{NH}_3$의 몰 수:
- 수소(H) 원자량 1이므로, $\text{H}$ 원자 $6 \text{ g}$은 $\mathbf{6 \text{ mol}}$이다.
- $\text{NH}_3$ 분자 1개에는 $\text{H}$ 원자가 3개(3몰) 들어있다.
- $\text{NH}_3$의 몰 수($x$)의 3배가 수소의 몰 수(6 mol)이므로, $x \times 3 = 6$.
- 따라서 $\text{NH}_3$는 $\mathbf{2 \text{ mol}}$이 있어야 한다.
- 이와 같은 몰-질량-개수 변환 및 구성 원자 계산을 암산으로 빠르게 할 수 있도록 연습하는 것이 이 단원의 핵심이다.
'Chemistry > 일반' 카테고리의 다른 글
| 6. 몰 농도 (몰 농도 용액 만들기, 용액 묽히기) (0) | 2025.11.16 |
|---|---|
| 5. 화학 반응식과 몰 농도 (화학 반응식, 퍼센트 농도, 농도, 몰 농도) (0) | 2025.11.16 |
| 4. 화학식량과 몰 (몰과 기체의 부피 사이의 관계, 몰과 화학 반응식) (0) | 2025.11.16 |
| 2. 탄소 화합물의 유용성 (0) | 2025.11.16 |
| 1. 화학의 유용성 (0) | 2025.11.16 |



